阴离子层析的病毒去除表现以及影响因素
病毒污染是使用源自哺乳动物细胞系的生物技术产品的潜在风险。生产过程中,无论处于临床前非GMP、临床GMP或商业化阶段,均可能受到内源性或外源性病毒的污染,对患者安全构成严重威胁。据统计,过去36年间共报告了26起哺乳动物细胞培养物的病毒污染事件,其发生在产品生命周期的所有阶段。因此,确保产品病毒安全性是行业监管与工艺开发的核心关注点。
为了保证这些产品在潜在病毒污染方面的安全性,监管机构要求进行病毒清除研究,以评估纯化过程清除内源性和外源性病毒的能力。一般来说,下游工艺减少病毒是通过柱层析和专用的病毒去除步骤(即低pH值孵育、去污剂处理和纳滤)来实现的。本文将简述阴离子层析(Anion exchange chromatography, AEX)病毒去除效果及影响因素。
AEX病毒去除机理与能力
在下游纯化工艺中,层析步骤除有效去除工艺相关杂质和产品相关杂质外,亦是重要的病毒清除单元操作。其中,AEX常被证明是病毒清除最为关键的步骤。
AEX病毒去除机理
AEX用于抗体类项目纯化时,主要采用两种模式:
• 流穿模式 (Flow Through Mode, FT):此模式利用目标单抗与模型病毒等电点(pI)的差异。多数单抗pI较高,在适宜的缓冲液条件下(pH 7.0~8.5,低电导率),单抗因带正电荷而流穿;而模型病毒(如X-MuLV pI~5.8, MVM pI~6.2)在此条件下带负电荷,通过与填料带正电荷的配基发生静电吸附而被去除。
• 结合-洗脱模式 (Bind and Elute Mode, B/E):此模式则利用单抗与病毒在结合力强度上的差异。在特定条件下,单抗和病毒均结合至填料上,随后通过改变洗脱条件,选择性地洗脱单抗,而病毒仍保留在填料上。
AEX色谱病毒去除能力
大量数据库数据显示,FT模式AEX能有效去除包膜病毒和非包膜病毒,统计数据表明(如Fig.1):
• 约70%的AEX应用采用FT模式,约30%采用B/E模式。
• FT模式对两种病毒表现出较高的稳健性,且批次间变异性较低。
• B/E模式对两种病毒的清除能力呈现更高的批次间变异性。
• 两种模式下细小病毒批次间变异性均大于逆转录病毒。
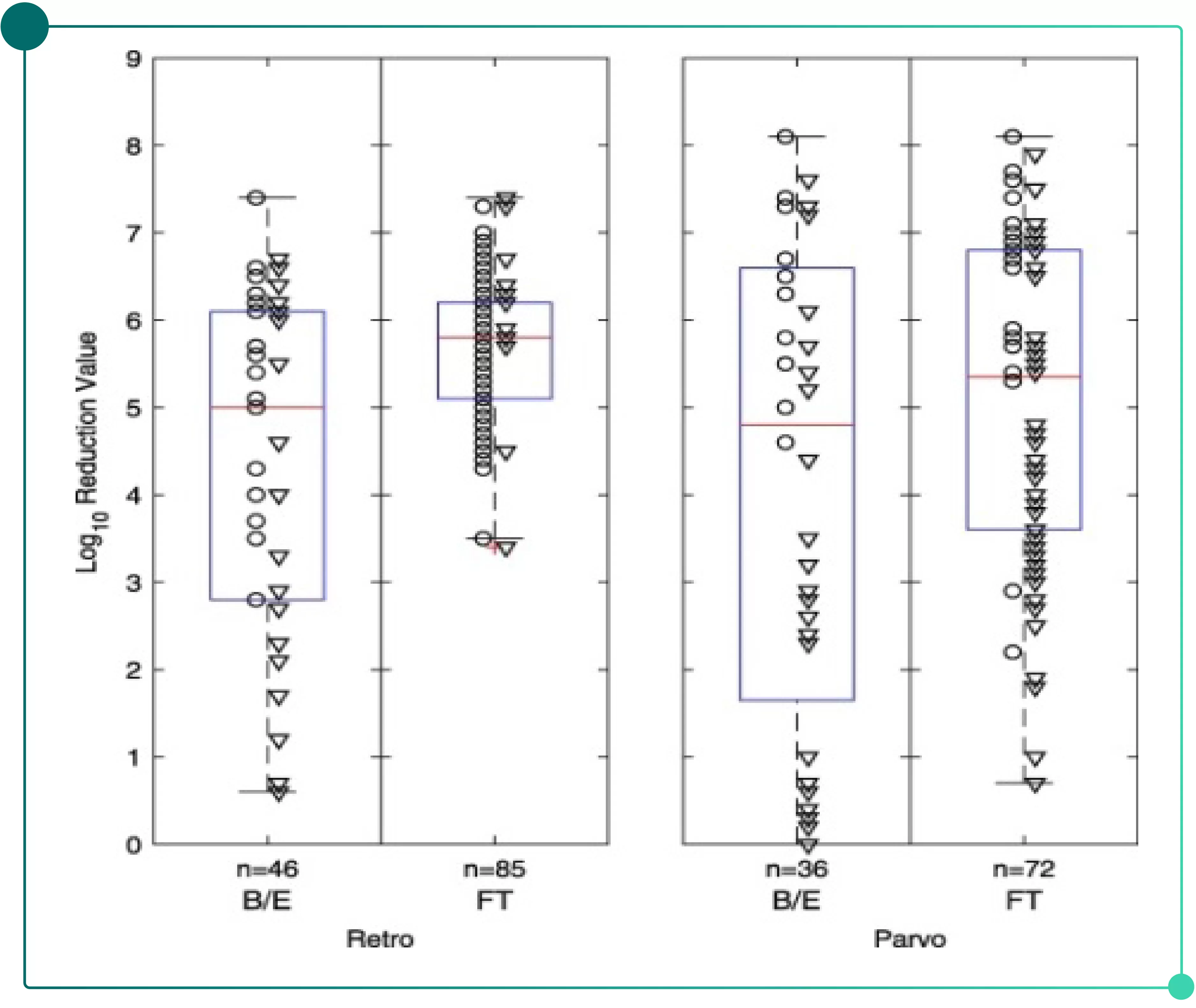
Fig.1 阴离子交换层析对逆转录病毒和细小病毒的去除能力总结(FDA数据库统计)
复合模式阴离子层析病毒去除能力
复合模式层析填料同时具有离子交换与疏水相互作用等多种作用力,这种多模式机制赋予了其独特的优势:
• 增强缓冲液的兼容性:可在更宽的pH值和电导率范围内有效运行。
• 更稳健的病毒清除:如Fig.2所示,与单一模式AEX相比,复合模式AEX在高盐条件下仍能维持优异的细小病毒去除效能(在高盐区仍保持较高LRV)。
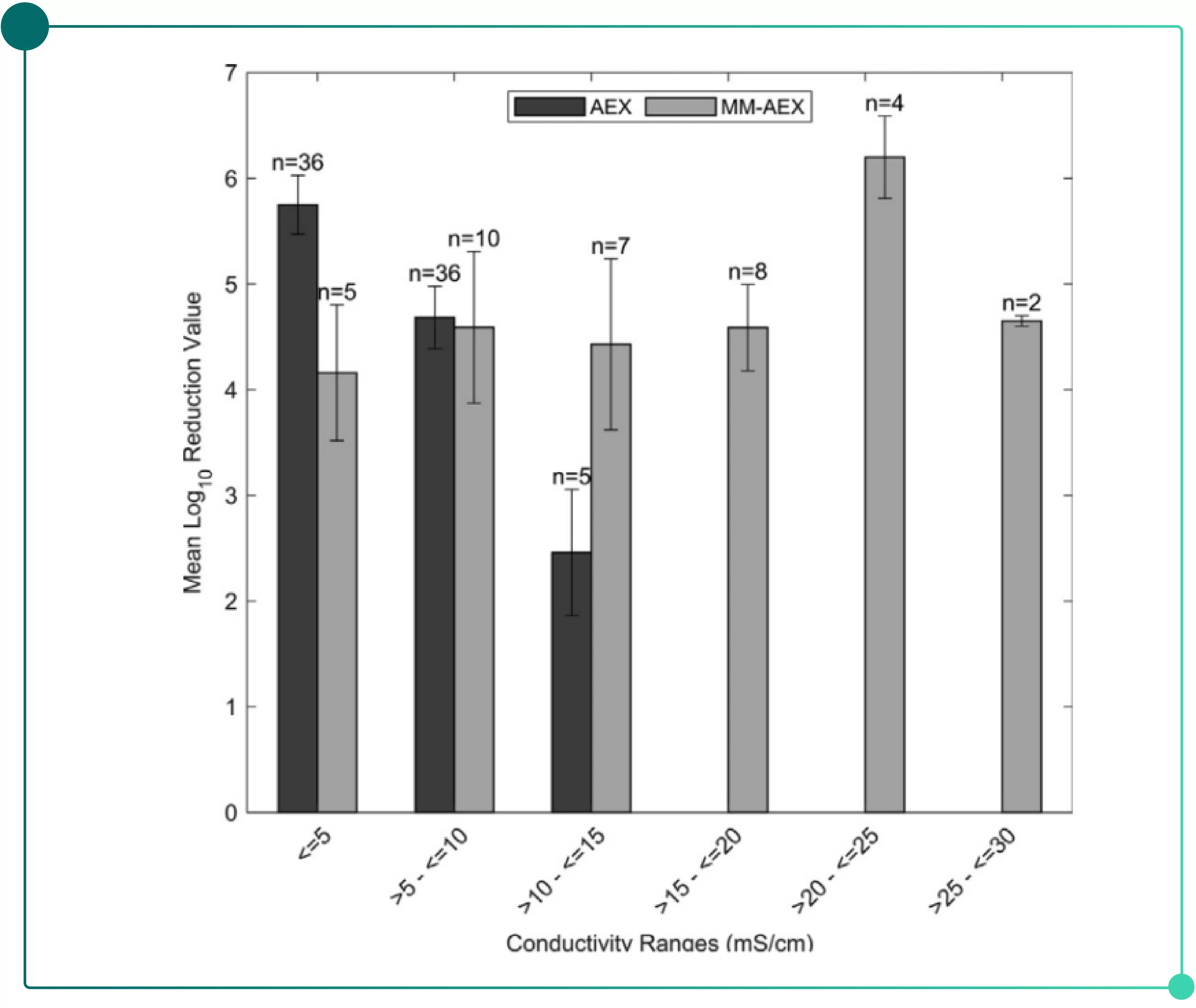
Fig.2 复合模式阴离子层析 vs. 单一阴离子层析对细小病毒的去除能力比较(FDA数据库统计)
AEX病毒去除能力的关键影响因素
病毒-介质相互作用强度可能受到病毒等电点(pI)与溶液pH值、溶液盐浓度、Mab性质、病毒上可用结合位点的数量以及竞争物存在等因素相互作用的的影响。
• pH值:病毒-AEX的相互作用为静电,但在低盐条件下,X-MuLV在不同pH下清除效果比较稳定,X-MuLV和AEX填料之间的相互作用在5.0~8.0的范围内仅略微依赖于pH值。与X-MuLV 清除率不同,不同pH值的MVM(pI 6.2)去除符合预期,当50 mM氯化钠的pH值从5增加到8时,LRV大约增加4。
• 离子强度:对于单一的阴离子层析,通常随着盐浓度增加,病毒去除效果逐渐降低。而复合模式层析受盐浓度影响较小,由Fig.2可知。
• Mab性质:对于任何给定类型的色谱分析,特定病毒的清除率不仅受色谱形成条件的影响,还受目标mAb本身的影响,病毒可以通过其表面负电荷与带正电荷的mAb相互作用,从而影响病毒的去除效果。
• 病毒种类:X-MuLV的pI为5.8,该现象(X-MuLV在pH值为5时与AEX介质结合)是不正常的,表明该病毒在该pH值时其表面仍旧含有带负电荷的斑块。可知pI是预测病毒等大型复杂结构与离子交换(IEX)填料相互作用是不足的。相反,在确定病毒-IEX 填料相互作用方面,病毒表面电荷分布比 pI 更相关。
综上可知,阴离子层析对病毒的去除效果受到多种因素影响,因此为获得稳健的病毒清除效果,单一模式阴离子层析建议pH 值为7.0~8.5、电导率<10 mS/cm和载量<100 mg/ml。
博格隆阴离子填料病毒去除能力数据
复合模式阴离子填料 Diamond MIX-A
• 高效清除能力:在某项目中,针对多种包膜和非包膜病毒模型(X-Mulv, MVM, PRV, Reo3)Diamond MIX-A展现出优异的清除能力,LRV范围达4.5-5.34 log。
• 卓越耐盐性:在极具挑战性的高盐条件下(上样电导22 mS/cm, pH 6.43, 载量~60 mg/mL),保留时间(5 min),Diamond MIX-A对X-Mulv仍实现了显著的清除效果,LRV分别达到3.04 log、3.25 log,验证了其在高盐环境下的稳健性。
强阴离子交换填料Diamond Q系列
下表汇总了Diamond Q系列填料在多个单抗项目中对模型病毒X-MuLV和MVM的清除表现:
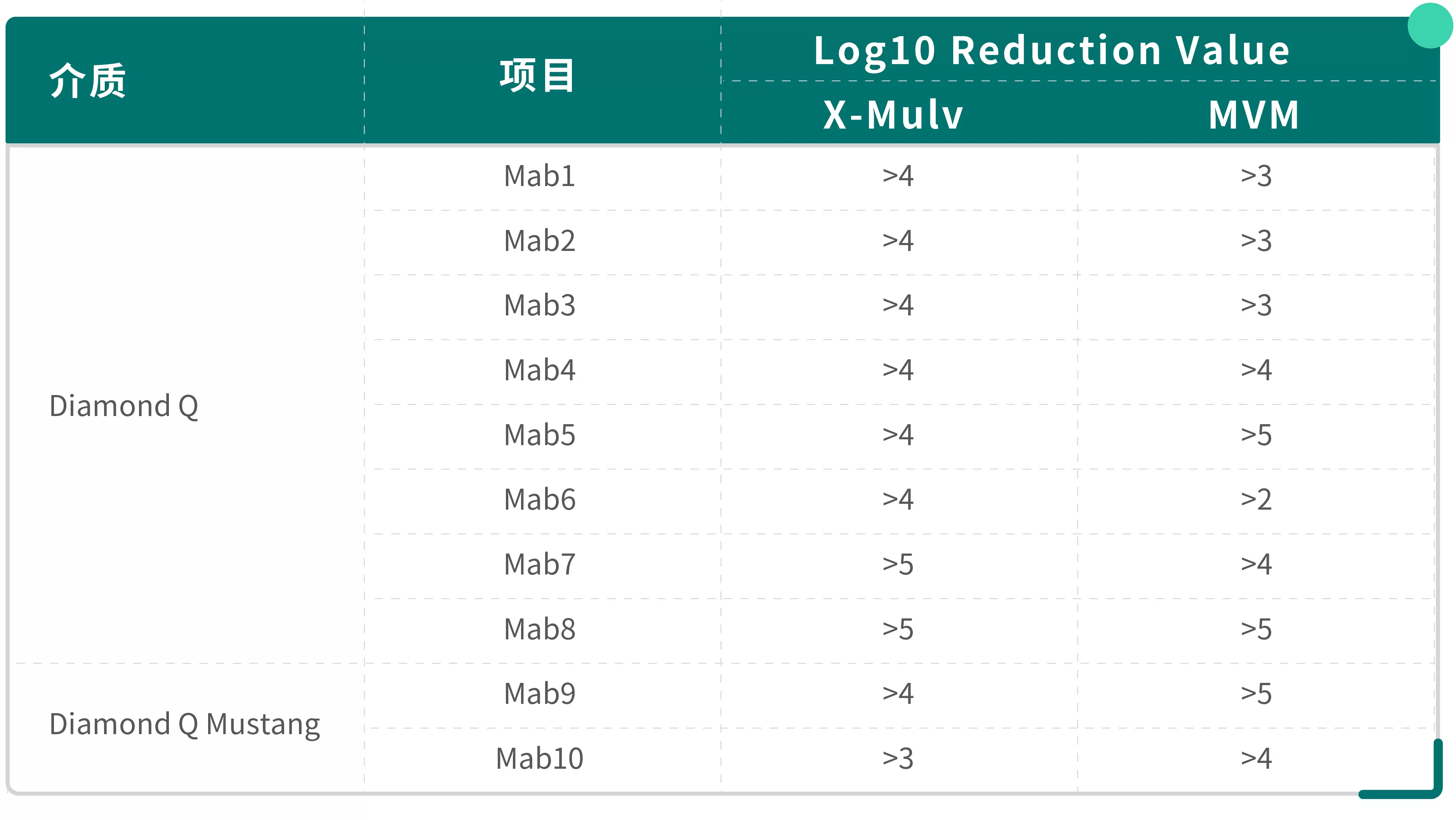
• Diamond Q对逆转录病毒X-MuLV展现出高度一致且优异的清除能力(所有项目LRV≥4 log)。
• 对细小病毒MVM的清除能力存在一定的项目间变异性(LRV范围从2~5 log),这也印证了前文所述。尽管如此,在多数项目中仍能达到≥3 log的有效清除。
• Diamond Q Mustang 在测试项目中同样表现出良好的病毒清除能力。
总结
下游纯化工艺中各层析步骤在病毒清除方面具有不同的能力和稳健性水平。阴离子交换层析(AEX),尤其是流穿模式(FT),已被广泛证明是清除病毒的关键单元操作。
然而,即使是通常被认为稳健的AEX步骤,其清除效果(特别是对细小病毒)也可能因目标Mab的特异性、工艺参数的选择而存在差异。复合模式AEX填料(如Diamond MIX-A)因其结合了多种作用力,在高盐条件下展现出更稳健的病毒清除性能。
为确保病毒清除的稳健性,需在经过验证的操作参数范围内运行AEX。病毒清除研究应使用代表性的模型病毒,并在工艺最差条件的情况下进行,以充分证明该步骤在各种潜在风险场景下均能提供可靠且符合监管要求的病毒去除能力。
参考文献
[1] Barone, P.W., et al. Viral contamination in biologic manufacture and implications for emerging therapies. Nat Biotechnol 38, 563–572 (2020). (Updates the scope and context of viral risk).
[2] Ajayi, O.O., et al. An updated analysis of viral clearance unit operations for biotechnology manufacturing. Curr Res Biotechnol 4, 190-202 (2022). (Provides a modern overview of unit operations, including AEX).
[3] Cai, K., et al. Virus removal robustness of ion exchange chromatography. Biologicals 60, 64-70 (2019). (Specifically addresses robustness factors for IEX virus clearance, critical for the discussion on variability).
[4] Li, Y. Viral removal by column chromatography in downstream processing of monoclonal antibodies. Protein Expr Purif 198, 106131 (2022). (Focuses on chromatography for mAbs, directly supporting the application context).
.png)


