阳离子交换层析在ADC纯化中的应用
一、引言:抗体偶联药物—肿瘤治疗的“生物导弹”
抗体偶联药物(Antibody–drug conjugates,ADCs)被誉为肿瘤治疗的“生物导弹”,通过抗体靶向肿瘤细胞,精准释放细胞毒性载荷,极大提升了疗效并降低系统毒性。
自2000年首款ADC药物Mylotarg上市以来,全球已有超17款ADC获批(截止到2024年),覆盖血液瘤和实体瘤,市场估值超百亿美元。而ADC的复杂结构(由抗体、连接子及有效载荷组成,如Fig.1所示)对生产工艺提出了极高要求。本文将聚焦阳离子交换层析在ADC高效纯化中应用。
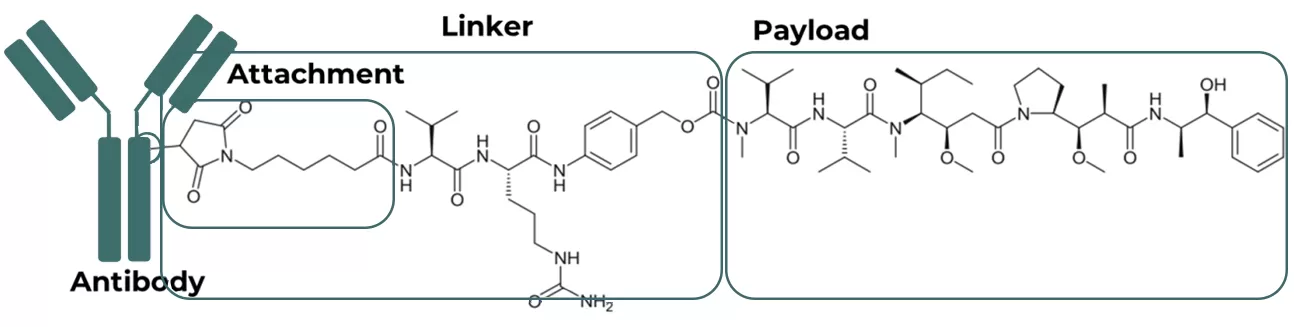
Fig.1 Anti-CD30 MMAE conjugate (brentuximab vedotin; Adcetris®)结构
二、 抗体偶联药物质量属性简述
生物制品工艺开发的核心目标在于构建稳健可控的生产工艺体系,确保可重复制备出符合预设质量属性的优质产品。对于传统非抗体偶联药物(Non-ADC biologics),其关键质量属性(Critical Quality Attribute, CQA)包括可能影响临床安全性与有效性的关键指标,如产品大小相关变异体(如聚集体、片段)、电荷异质性、氧化变体等,工艺相关杂质(宿主细胞蛋白、DNA残留)、浓度、活性等。而抗体药物偶联物由于兼具生物大分子与化学小分子的双重特性,还需额外关注其他质量属性,包括药物抗体比率(Drug-to-Antibody Ratio, DAR)、DAR值的组成、游离毒素残留、偶联反应溶剂残留等。
游离毒素作为高风险工艺相关杂质。这类未偶联小分子因缺乏靶向递送机制,无法特异性作用于治疗靶点,未能提升疗效,可能会引发全身毒性风险。此外,工艺开发需同步关注偶联反应体系中引入的有机溶剂(如DMF、DMSO)、还原剂(如TCEP)等工艺相关杂质的清除效率,确保终产品符合质量属性放行要求。
三、阳离子交换层析在ADC纯化中的应用
1、阳离子层析去除游离毒素
结合-洗脱色谱法作为一种常规分离技术,可有效实现ADC中游离毒素的去除。该方法基于ADC与游离毒分子间显著的理化特性差异,通过选择性吸附实现高效分离。
在层析工艺中,首先对含有游离毒素及溶剂的偶联反应体系进行调节到目标上样条件,随后上样至色谱柱,借助离子相互作用选择性捕获ADC,游离药物及残余溶剂因缺乏有效结合位点而随流动相直接穿透。
但是部分色谱填料可能与非目标组分(如游离毒素)以及游离毒素可能与ADC存在非特异性相互作用。因此,建议进行系统化的填料筛选,必要时可引入强化淋洗步骤,以确保游离毒素的完全清除。
Fig.2展示了阳离子交换色谱通过结合-洗脱模式去除游离药物的典型流程。通过上样过程以及平衡缓冲液的持续淋洗可有效去除残留的游离毒素(游离毒素含量由52.2%降低至5.0%),从而实现游离毒素与ADC高效分离。
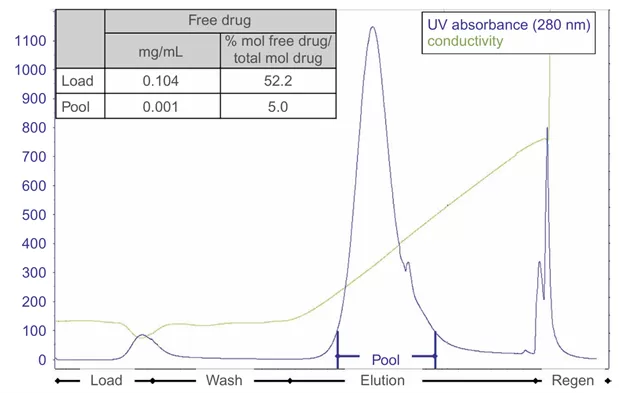
Fig.2 阳离子交换层析纯化图谱
Table 1. 阳离子交换层析纯化方法

2、阳离子层析去除聚集体
ADC产品工艺的复杂性,决定了其在偶连工艺结束后可能会导致聚集体含量升高至不可接受的水平,因此在偶联后引入纯化步骤可能是必要的,以确保该工艺能够满足所需产品质量要求。
对此可采用阳离子结合-洗脱色谱法,可有效实现ADC中聚集体的去除。如下所示,该方法基于聚集体与单体的理化特性差异实现高效分离,该ADC采用还原链间二硫键后偶联,纯化方法如下:
• A液90mM NaAC-HAC,pH5;
• B液400mM NaAC-HAC,pH5;
• 载量60mg/mL;
• 洗脱0→100% B液,20CV线性梯度洗脱,分段收集,结果如下所示,可知阳离子层析可以有效去除ADC中残留的聚集体。
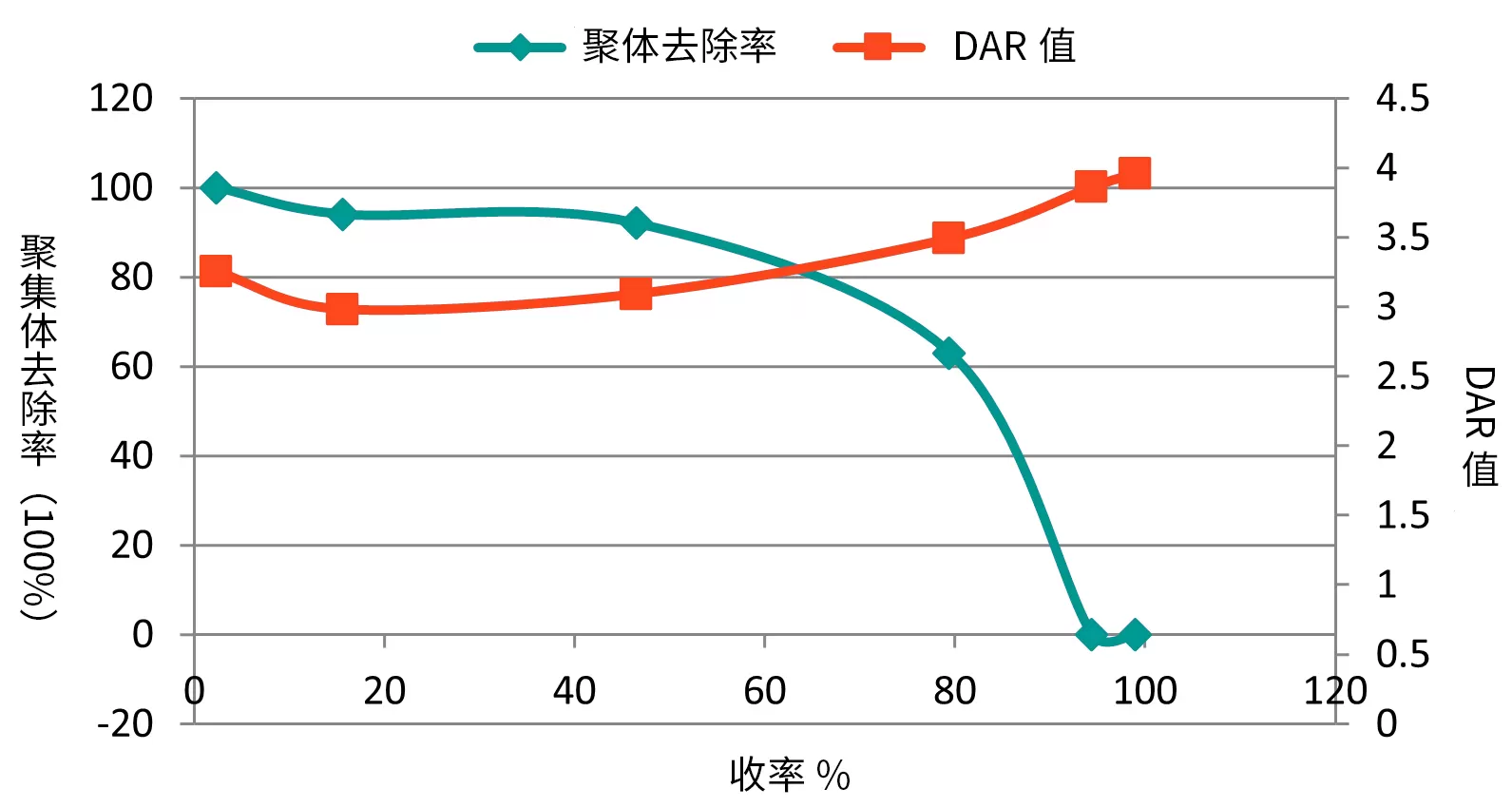
Fig.3 阳离子交换层析聚集体去除结果
四、博格隆阳离子层析介质
博格隆公司创新研发的Diamond CD-S阳离子填料不仅适用于单克隆抗体、双特异性抗体、融合蛋白等的精细纯化,也可满足ADC生产工艺中游离毒素以及聚集体去除的要求,其具有如下技术优势:
1、高动态结合载量,其在高盐浓度下仍具有较高的动态结合载量(10%DBC可达100 g/L,如下图所示);
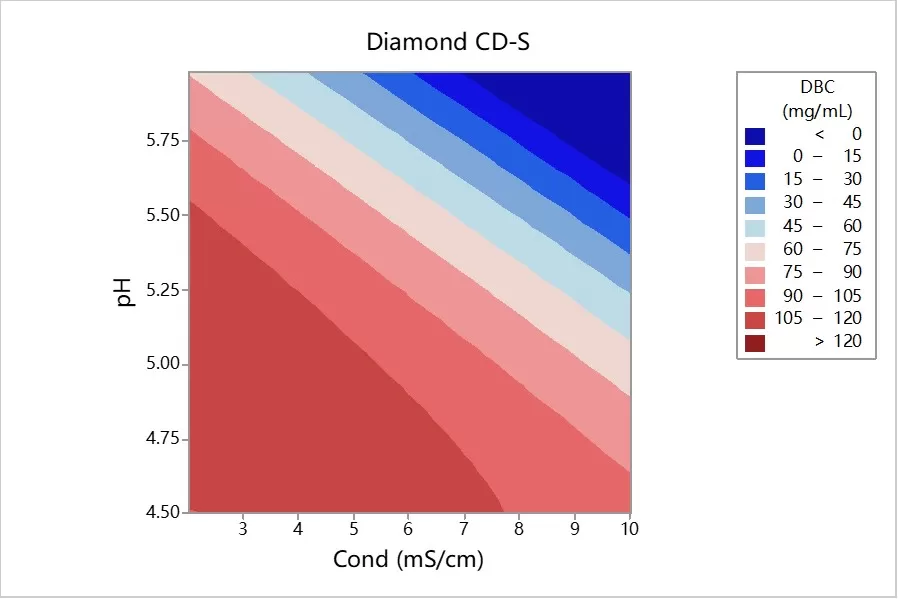
Fig.4 阳离子交换层析Diamond CD-S 动态结合载量图
2、采用高刚性琼脂糖微球,具有高流速、低反压特点,更适用于产业化,耐压5bar;
3、优异分辨率、稳定的批间一致性;
4、良好的有机溶剂耐受性(15% DMSO加速40℃加速7天稳定性良好),可用于ADC产品纯化。
此外,博格隆提供的Diamond SP Mustang等系列阳离子交换层析产品,可完整覆盖从裸抗精细纯化到ADC纯化的工艺需求。
参考文献:
[1] Dumontet, Charles , J. M. Reichert , and L. A. Beck . "Antibody-drug conjugates come of age in oncology." Nature reviews Drug discovery 22.8(2023):641-661.
[2] Hutchinson, Matt H., et al. "Process development and manufacturing of antibody-drug conjugates." Biopharmaceutical processing. Elsevier, 2018. 813-836.
[3] Hendricks, Rachel , et al. "Simplified strategy for developing purification processes for antibody-drug conjugates using cation-exchange chromatography in flow-through mode." Journal of chromatography, A: Including electrophoresis and other separation methods 1666-(2022):1666.
[4]刘慧芳等. "一种抗体偶联药物的阳离子交换层析纯化方法.", CN104208719A. 2014.






.png)


