从滴度跨越到工艺强化:为何柱层析依然是抗体纯化的压舱石?
回望来时:从 50 mg/L到10 g/L 的四十年剧变
2026年的今天,生物制药领域一片蓬勃:单克隆抗体(monoclonal antibody,mAb)百花齐放,以单抗为骨架的双抗、ADC(antibody-drug conjugate,抗体药物偶联物)、AOC(antibody-oligonucleotide conjugate,抗体寡核苷酸偶联物)等产品被药监机构大量批准或处于临床阶段。
然而,这种繁荣其实只有短短四十年,四十年前生物制药几乎还是一片荒漠。就在1986那年,强生公司开发的第一个单克隆抗体OKT3获批上市,正式开启了抗体药物的黎明时代。但当时技术仍显稚嫩:抗体筛选高度依赖杂交瘤技术,基因拷贝数低,培养基大多含血清,CHO细胞没有被大量应用,细胞比生产率(qp)低,峰细胞密度也不高,积分活细胞密度(integral viable cell concentration)同样有限,导致表达量大多仅维持在10~50 mg/L的水平(Walsh & Walsh, 2022)。表达量低这一现实,决定了当时下游纯化的主要压力在于微量抗体的有效捕获,而上游培养规模并非主要矛盾。
然而,随着DHFR(dihydrofolate reductase,二氢叶酸还原酶)和GS(glutamine synthetase,谷氨酰胺合成酶)扩增系统的成熟,细胞株经加压筛选后GOI(gene of interest,目标基因)拷贝数大幅增加;定点转座技术进一步提升了GOI转染效率;培养基也历经迭代,从含血清培养基发展到含有限蛋白质培养基,直至如今占据主导地位的CD(chemically defined,化学成分限定)培养基,为精确调控细胞培养提供了可能;补料分批培养(Fed-batch)则实现了对细胞代谢流的相对精准调控……这些进步共同推动上游细胞培养表达量在过去四十年间实现了指数级跃升。
如今,行业内大多数抗体滴度已稳定达到5–10 g/L,甚至在强化灌流工艺中逼近20 g/L(Liang et al., 2023);培养规模也从2,000 L逐步扩大至5,000 L甚至20,000 L。上游产能爆发极大降低了抗体单位成本,抗体药物的COG(cost of goods)持续下降。但与此同时,下游纯化却面临巨大压力。一方面,受限于液体分配和柱管耐压,工业上最大层析柱直径仅两米,常规装填体积不到1,000 L;另一方面,下游自动化程度远低于上游,大量操作仍需手动完成。这两重限制叠加之下,一个表达量为10 g/L的万升反应器,给下游带来的负荷可想而知。

Fig.1 典型单克隆抗体下游工艺
典型单克隆抗体下游工艺首先采用蛋白 A 层析进行捕获,随即进行病毒灭活,然后通过两种不同的纯化方法对产物进行精纯。最后通过纳滤步骤实现病毒去除,同时对原液进行浓缩与配制。
下游工艺的三条突围路径
为了承接住上游细胞培养越来越高的表达量和越来越大的培养规模,下游工艺并没有停滞不前,而是沿着三个方向进行不断进步:
◉ 方向一,单品进化:高载量、高耐压、高流速填料
这一思路简单直接且行之有效:既然上游产量大幅提升,下游也需同步升级,包括扩大层析柱直径以容纳更多填料。而更重要的是,在真正起纯化作用的填料上下功夫。填料厂商通过几十年持续不断的研发,不断对细菌的Protein A蛋白的结构域进行修饰、替换和重组,不断刷新动态结合载量(dynamic binding capacity,DBC)。同时,对于填料的基架,也通过不同的技术手段不断提高其耐压性能,使其可以耐受工艺上的高流速,极大的提高了料液处理的通量,大幅缩短工艺时间,大规模的节省了厂房、设备等的占用,这对于CDMO公司来说尤为重要,因为可以挤出更多的Slot(生产时段)。
博格隆公司Protein A 系列填料经过多年的持续研发、迭代,搭配耐高压力的Diamond基架,可保障用户在更高流速、更短的保留时间内处理完料液,目前有多款商业化的产品可提供给客户使用。比如,在确保耐碱性和长寿命的前提下,新型 Extrem A Diamond 填料,在6min 保留时间的载量已逼近 80 mg/mL,如 Table 1 所展示。
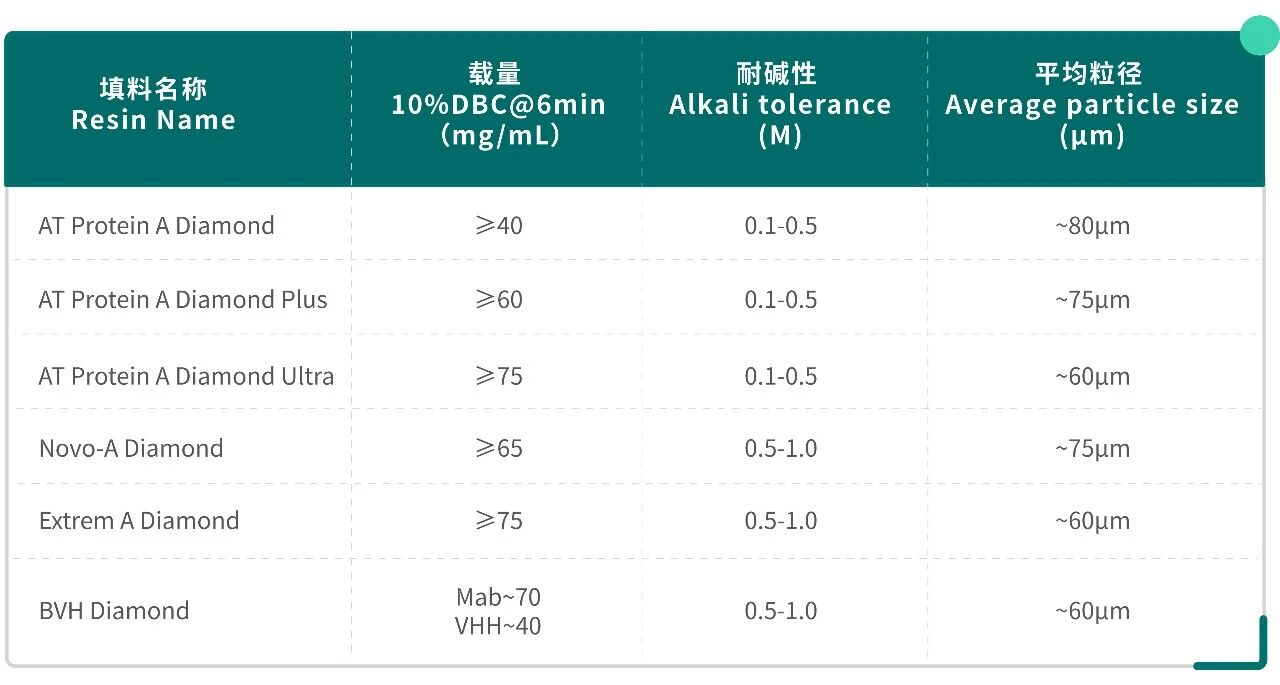
Table 1. 博格隆 Protein A 系列填料
目前,应对上游高滴度带来的产能压力,主流药企普遍采用是这种提升单位体积效率的策略:通过提高填料载量、缩短保留时间,来增加每升填料在单位时间内处理的料液量。
◉ 方向二,提高填料利用率:连续流工艺
连续生产已广泛应用于石油化工、冶金精炼、汽车制造等众多行业。近年来生物制药行业也开始加大对连续生产的探索,美国FDA在2019年发布官方声明推动生物制药的连续制造,并颁布了质量控制指南。目前,连续灌流细胞培养技术已经得到突破,并逐渐普及。在上游培养实现连续化的情况下,下游分离纯化就成为整个生产过程的关键限速步骤。因此,这一方向的核心是:与其单纯扩大柱体积,不如采用小体积柱子,最大限度利用填料每一份载量,并提升周转速率。
这个思路之所以可行,是因为传统柱层析留下的bug:填料实际上样的载量低于饱和载量。其原理可简述如下:Fig.2(a)为典型的抗体穿透曲线,为避免产品损失,常规柱层析通常在较低穿透点上样(常按10%穿透载量再打八折)。例如,若测得10%穿透载量为100 mg/mL,工艺中实际使用载量可能仅为80 mg/mL。此时填料并未完全饱和,利用率一般仅为50%~60%,相当于Fig.2(a)中仅利用了A部分载量,造成Protein A填料的浪费。为提升填料利用率,可将单柱批次模式(Fig.2(b))转变为多柱串联连续上样模式(Fig.2(c)):柱1穿透的抗体被后续柱2捕获,持续上样至时间t₂,此时柱1填料载量达到(A+B),利用率可优化至90%以上;柱1吸附完成后,与柱2断开,料液切换至柱2继续上样,而柱1则依次进行冲洗、洗脱、再生和平衡,随后重新串联,循环操作,从而实现料液连续上样(Jing et al., 2021; Steinebach et al., 2016)。
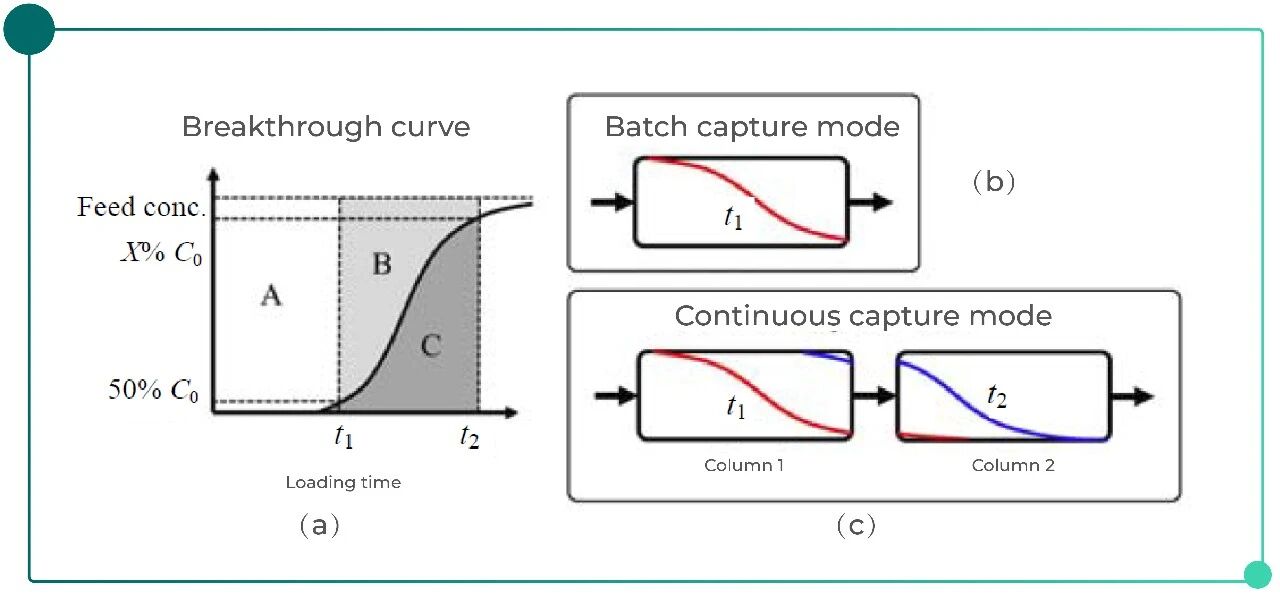
Fig.2 连续捕获层析原理图
目前市场上有多种连续流设备及其控制、模拟系统,实际操作远比上述简化原理复杂(Jing et al., 2021)。
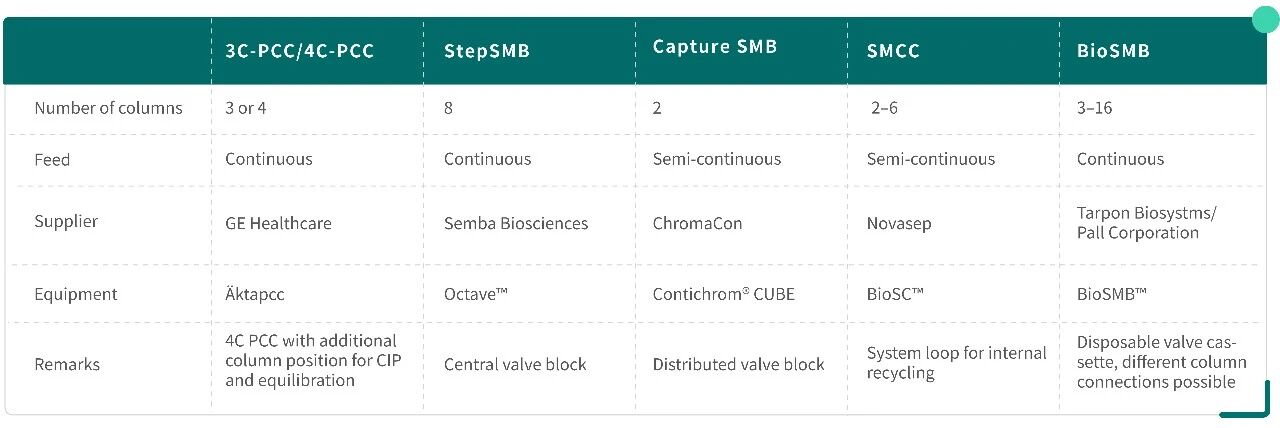
Table 2. 蛋白捕获阶段各类连续流设备汇总
整体来说,连续流层析模式较多,操作复杂,过程参数多,优化设计较为困难;在连续流处理中,料液连续输入,产品连续输出,其中任一环节出现异常都将是灾难性的,这些是其目前未能大规模应用的主要障碍(Jing et al., 2021; Steinebach et al., 2016)。
◉方向三,对流速的极致追求:膜层析
对流速的极致追求,造就了膜层析。这就是第三个解决思路:若无法进一步提升单品载量或运转效率,那就全力加快处理速度。膜层析(membrane chromatography)的基质通常是堆叠的多孔薄膜,厚度通常在毫米级,膜上修饰有特定的配基(如阴离子交换配基Q)。料液在压力驱动下以高流速通过膜孔道。传统柱层析依赖填料颗粒内部的扩散传质(diffusion),单抗等大分子需要较长时间才能扩散到配基结合位点;膜层析利用对流传质(convection)机制,目标分子在流动过程中直接与膜孔道表面的配基快速接触并结合,几乎无需依赖缓慢的分子扩散,这就可将原本数小时的柱层析缩短至分钟级(Boi et al., 2020)。
知去处:为什么柱层析依然无可替代?
尽管膜层析和连续流制造近些年被炒得火热,但在真实的工业生产线,尤其是 2000L 以上规模中,传统柱层析依然稳如泰山。其原因在什么地方呢?
◉首先是载量
膜层析在捕获(如单抗的Protein A亲和捕获)时,膜的有效结合面积远不及具有深邃孔径结构的传统填料。传统填料颗粒(beads)通过内部多孔结构,提供巨大比表面积,结合位点丰富,载量更高,例如博格隆公司Diamond Q的动态结合载量出厂标准大于100 mg/mL。而膜层析主要依赖表面吸附,单位体积可用结合位点较少,动态结合载量通常仅为填料的30–60%。Boi et al. (2020)的直接对比实验(相同3 mL体积、相同Q配基)显示,在相同的流速下,柱层析的动态结合容量(10%穿透)为62.8 mg/mL,而膜层析仅为20.7 mg/mL。这意味着要达到同等载量,膜需显著增加体积或层数,从而大幅推高单次投入的膜材料成本。
◉其次是使用寿命
膜层析通常设计为一次性使用或仅能使用数次。这虽然避免了传统填料所需的清洗、再生及潜在的污染风险,但也带来了较高的初始材料成本,摊销后难以与Protein A填料竞争。相比之下,填料具有良好的长期稳定性,可重复使用多次,其成本得以分摊,从而显著降低了每克产品的纯化成本。
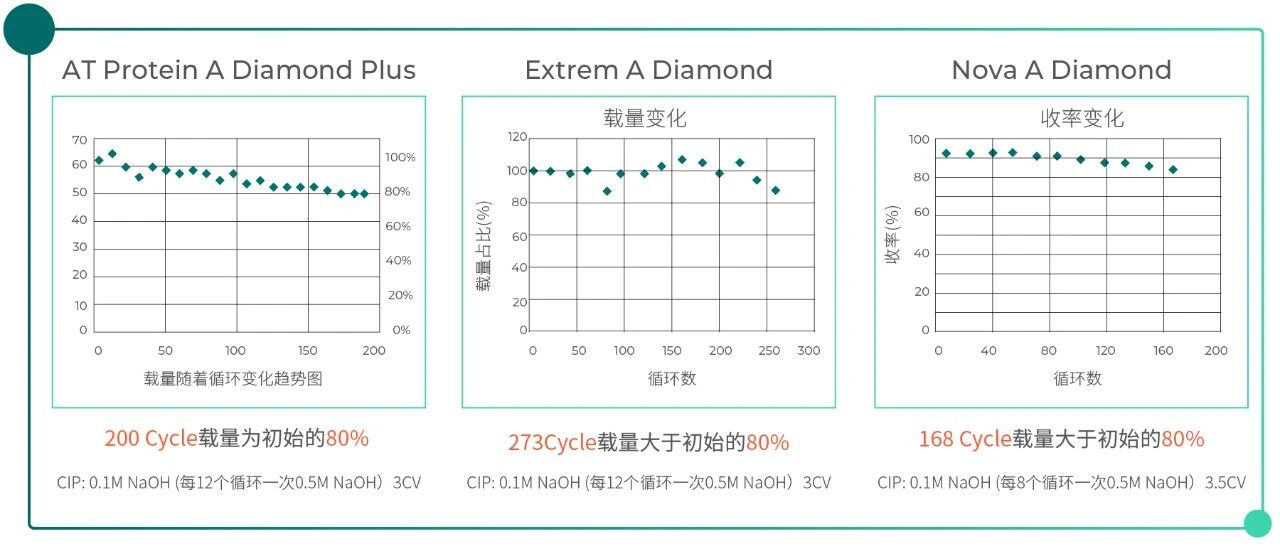
Fig.3 博格隆公司亲和填料使用次数超过数百次
◉再者是纯化的分辨率
抗体的质量控制对电荷异质性(酸性/碱性变体)和聚集体的去除要求极为严苛。这些杂质直接影响产品纯度、安全性和疗效。以填料为核心的柱层析凭借较高的柱床和数千个理论塔板数(N),显著提升分辨率(Rs),分辨率公式如下:
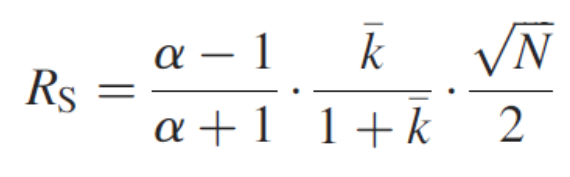
其中,N(理论塔板数)是柱效的核心,Rs与N的二次方根成正比。常规的长柱床使N大幅增加,从而实现精细的梯度洗脱,有效分辨细微的电荷差异或大小/疏水性差异,高效去除目标杂质。
相比之下,膜层析流路极短,通常仅数毫米,虽然传质快,但有效分离路径有限,理论塔板数远低于传统柱,难以提供高分辨率的梯度洗脱效果,尤其在精细分离电荷异质性和聚集体时表现受限,这从底层限制了膜层析的应用范围和规模。
总结
尽管连续流层析与膜层析在通量和工艺集成上确实优势明显,但在真实的工业规模抗体纯化中,上游滴度已跃升至10 g/L以上,培养规模也达到了万升级别。面对这样的挑战,传统柱层析拥有远高于膜层析的动态结合载量,可重复使用数百次的长寿命,以及柱床提供的数千理论塔板数所赋予的高分辨率,依然是保障高纯度、低成本与工艺稳健性的核心基石。
参考文献
[1]Steinebach F et al. Continuous counter-current chromatography for capture and polishing steps in biopharmaceutical production. Biotechnology Journal, 2016.
[2]Boi C et al. A direct comparison between membrane adsorber and packed column chromatography performance. Journal of Chromatography A, 2020.
[3]Jing S et al. 连续流层析及用于抗体分离的新进展. 高校化学工程学报, 2021.
[4]Walsh G, Walsh E. Biopharmaceutical benchmarks 2022. Nature Biotechnology, 2022.
[5]Liang et al. Enhancing and stabilizing monoclonal antibody production by Chinese hamster ovary (CHO) cells with optimized perfusion culture strategies. Frontiers in Bioengineering and Biotechnology, 2023.





.png)


