抗体纯化入门指南
抗体药物的高效生产,离不开一个精密而稳健的下游纯化工艺——它是连接上游表达与最终制剂的关键桥梁,也是控制产品质量与成本的核心阵地。本文将系统梳理抗体药物的基础知识,深入解析抗体下游纯化工艺的核心技术,为从事抗体药物研发和生产的人员提供一份完整的技术参考。
一、什么是抗体纯化
抗体纯化是从血清、细胞培养液、腹水等复杂生物样品中,利用抗体与其他物质的理化性质或结构差异,特异性分离、富集并提纯抗体蛋白的生物技术。其核心目的是去除样品中的杂蛋白、盐离子、细胞碎片等无关杂质,获得高纯度、结构完整且保持生物活性的抗体,是抗体制备、免疫检测、抗体药物研发与基础医学实验中不可或缺的关键步骤。在了解抗体纯化的方法和步骤前,我们先来了解一下抗体的结构以及分类。
二、抗体的结构与分类
1. 抗体的基本结构
抗体(Antibody),又称免疫球蛋白(Immunoglobulin,Ig),是机体免疫系统识别并中和外来抗原(如细菌、病毒)的关键效应分子。从结构上看,所有抗体单体均呈“Y”字形,由四条多肽链组成:两条相同的重链(Heavy Chain,H链)和两条相同的轻链(Light Chain,L链),通过二硫键连接形成一个对称的四肽链分子。
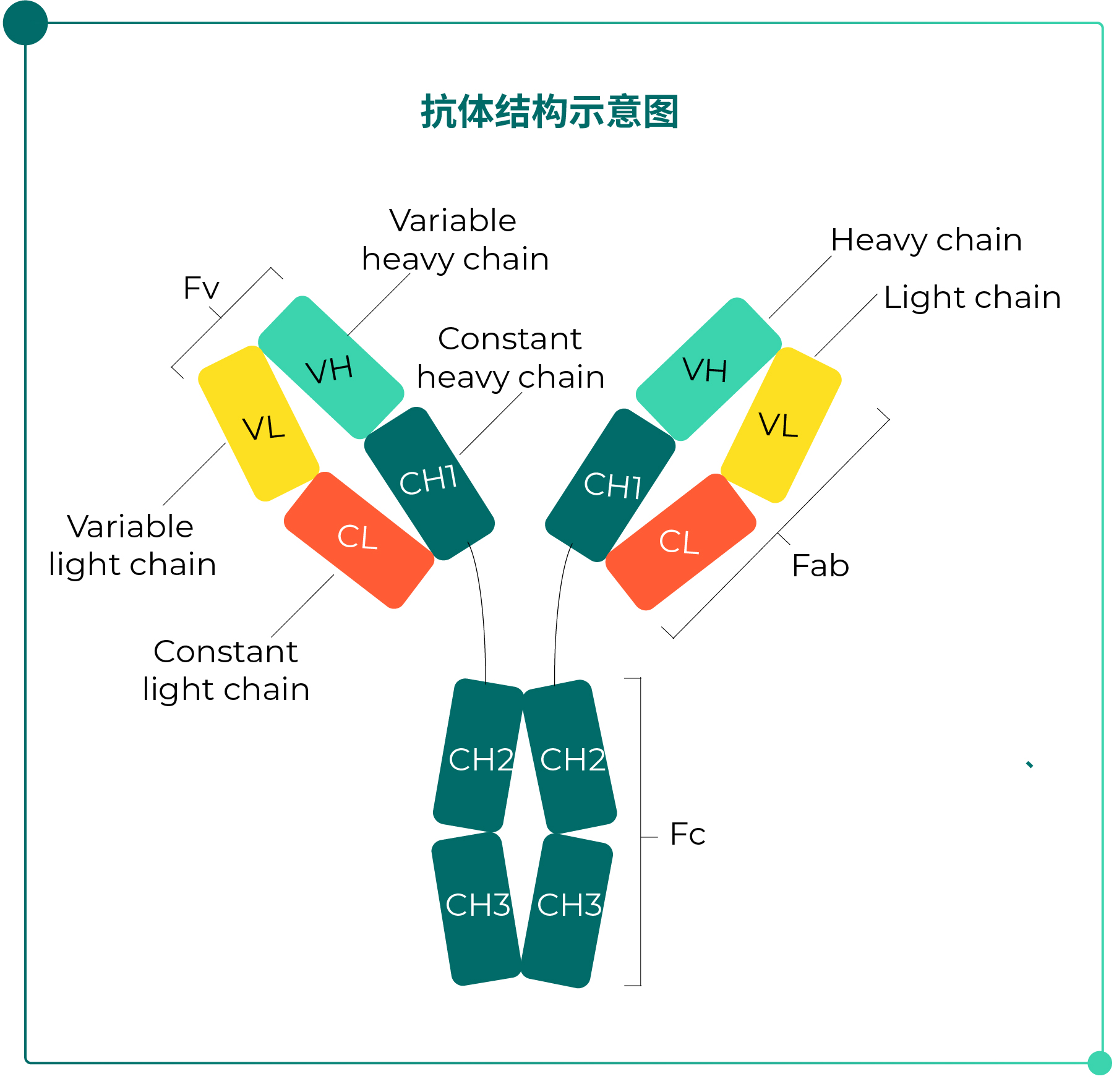
Fig.1 抗体结构示意图
轻链与重链:轻链由约214个氨基酸组成,分子量约24 kDa,分为κ型和λ型两个亚型;重链由450-550个氨基酸组成,分子量55-75 kDa,含有糖基化修饰。
功能区划分:每条轻链和重链均可进一步分为可变区(Variable region,V区)和恒定区(Constant region,C区)。V区位于肽链的N端,负责特异性识别和结合抗原;C区位于C端,序列相对保守,介导免疫效应功能。
抗原结合位点:V区中氨基酸序列高度可变的区域称为高变区(Hypervariable region,HVR),即互补决定区(Complementarity-determining region,CDR)。轻链和重链各有3个CDR,共同构成抗原结合位点,决定了抗体的特异性。
功能区与铰链区:抗体分子通过链内二硫键折叠成球形功能区(Domain),每个功能区约110个氨基酸。IgG、IgA、IgD的每条重链含有4个功能区(V区1个,C区3个),IgM和IgE的每条重链含有5个功能区(V区1个,C区4个)。铰链区(hinge region)位于IgG、IgA、IgD重链的CH1与CH2之间,富含脯氨酸,赋予抗体分子柔性,使其能够更好地与抗原结合。IgM和IgE则无经典铰链区。
2. 抗体的分类体系
根据重链恒定区氨基酸组成和排列顺序的差异,抗体可分为五大类:IgG、IgM、IgA、IgD和IgE,分别对应γ、μ、α、δ、ε五种重链。
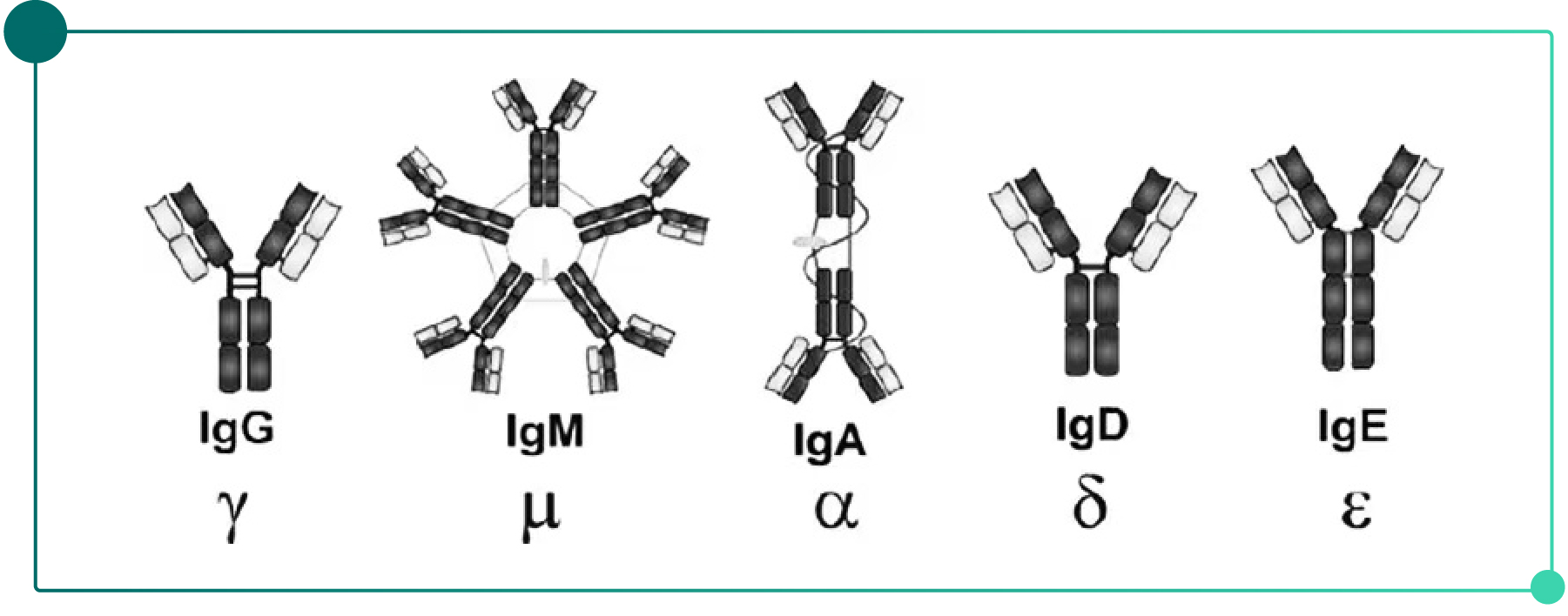
Fig.2抗体分类
IgG——治疗性抗体的主流形式:IgG是血清中含量最高的抗体,也是目前治疗性抗体中最常见的分子形式。根据铰链区结构和重链二硫键位置的差异,人IgG又可细分为IgG1、IgG2、IgG3和IgG4四个亚类。其中IgG1因其良好的效应功能和稳定性,成为绝大多数抗体药物的首选骨架。
IgM与IgA的特殊结构:IgM以五聚体形式存在,含有J链,分子量最大;IgA既可形成单体,也可通过J链形成二聚体,主要分布于粘膜表面。
轻链分型:根据轻链恒定区的差异,抗体分为κ(kappa light chain)型和λ(lambda light chain)型,据此,可将Ig分为两型(type),即κ型和λ型。
3. 抗体药物类型
根据分子结构特征,抗体药物主要分为以下四大类:
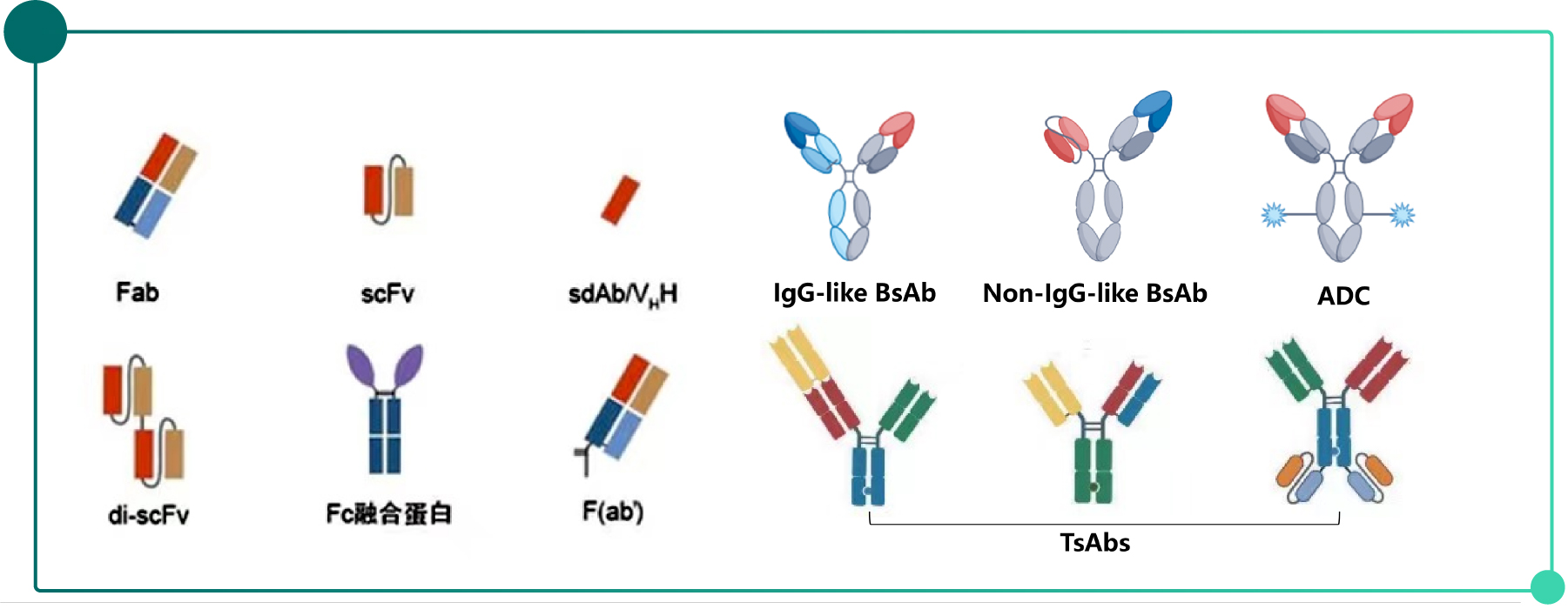
Fig.3 抗体药物的主流类型
(1) 片段类(Fc-free)
此类分子不含Fc区,主要通过抗原结合域发挥功能,分子量小、组织穿透性强。如Fig.3 左半部分:Fab抗原结合片段)、 F(ab')₂抗体片段、scFv单链可变区片段、di-scFv双链scFv、sdAb/VHH单域抗体/纳米抗体等。
(2) 单克隆抗体(Monoclonal Antibody, mAb)
单抗是抗体药物的基础形式,由单一B细胞克隆产生的同质抗体,结构为经典的IgG型(两条重链、两条轻链),含Fc区。
(3) 双特异性 / 多特异性抗体(Bispecific Antibody,BsAb / Multispecific Antibody,MsAb)
通过工程化设计,使单一分子能够同时识别两个或多个不同靶点,实现更复杂的生物学功能。比如IgG-like BsAb双抗、Non-IgG-like BsAb非IgG型双抗、TsAbs三特异性抗体等。
(4) ADC/XDC(抗体药物偶联物)
ADC由 IgG抗体 + 连接子(linker) + 小分子毒素(payload) 三部分组成。抗体靶向结合肿瘤细胞表面抗原,经内化后释放细胞毒性药物,实现精准杀伤,同时降低全身毒性。
XDC偶联药物家族拓展:随着技术发展,XDC(X-Drug Conjugate)已成为偶联药物的统称,涵盖RDC(放射性核素)、SMDC((小分子药物偶联物))、PDC(多肽)、AOC(寡核苷酸)、VDC(病毒样颗粒)、ISAC(免疫激动剂)、FDC(抗体片段)等多种形式。
三、抗体纯化的方法和流程
1. 抗体纯化的方法
层析技术是抗体纯化的核心手段。根据分离原理的不同,主要分为四大类,每类技术均有其独特的优势和适用场景。我们需要根据目的蛋白与杂质分子的特性分析,选择合适的纯化技术进行蛋白纯化。
|
目的蛋白与杂质特性差异
|
分离技术
|
|
特异性基团
|
亲和层析(AC)
|
|
等电点pI
|
离子交换层析(IEX)复合模式层析(MMC/MMA)
|
|
疏水性
|
疏水层析(HIC)复合模式层析(MMC/MMA)
|
|
蛋白大小
|
凝胶过滤层析(GF)
|
(1) 亲和层析(AC)——特异性基团
亲和层析是一种根据生物分子之间的特异相互作用来分离物质的层析方法,如酶和底物的结合、受体和配体的结合、抗体和抗原的结合等。这类结合既是特异的,又是可逆的。通过这种可逆的结合和分离来达到蛋白纯化的目的。亲和层析具有高选择性的特点,可快速从复杂体系中捕获目的蛋白,通常一步纯化就能达到90%以上的纯度;操作简便,适合作为第一步捕获工艺。
(2) 离子交换层析(IEX)——等电点pI
原理:离子交换层析是根据不同生物分子所带电荷性质和数量的差异来分离的一种层析技术。由于生物分子大都带有酸性基团或碱性基团,并且可以通过调节缓冲液的pH改变其带电性质和数量,生物分子与带相反电荷的阴离子交换填料或者阳离子交换填料相结合后,采用改变流动相中的离子强度或pH,让结合弱的先洗脱下来,结合强的后洗脱下来,从而达到分离纯化的目的。根据配基带电的不同分为阴离子交换层析(AEX)和阳离子交换层析(CEX)。
(3) 疏水相互作用层析(HIC)——疏水性
原理:疏水作用层析是根据分子表面疏水性差别来分离蛋白质或多肽等生物大分子的一种较为常用的方法。选择疏水作用层析填料的关键在于选择合适疏水强弱的配基,若蛋白质的疏水性较强就需要选择较弱的疏水填料,反之亦然。
(4) 凝胶过滤层析(GF)——蛋白大小
原理:凝胶过滤是一种根据生物分子的大小及形状来分离物质的层析方法,凝胶过滤介质为多孔的网状结构,生物分子越小进入介质内部越深,故在介质中的停留时间越长。每种介质的孔径都有一定的范围,选择凝胶过滤介质关键在于选择合适的分离范围,其次要考虑介质的机械性能和可放大性。
2. 抗体纯化的流程
一般抗体纯化的方法和流程包括捕获阶段(如Protein A/G/L亲和层析)和精纯阶段(离子交换、凝胶过滤层析、疏水作用等层析)等,最终获得高纯度抗体产物。典型的抗体纯化工艺流程包括以下几个核心单元操作:
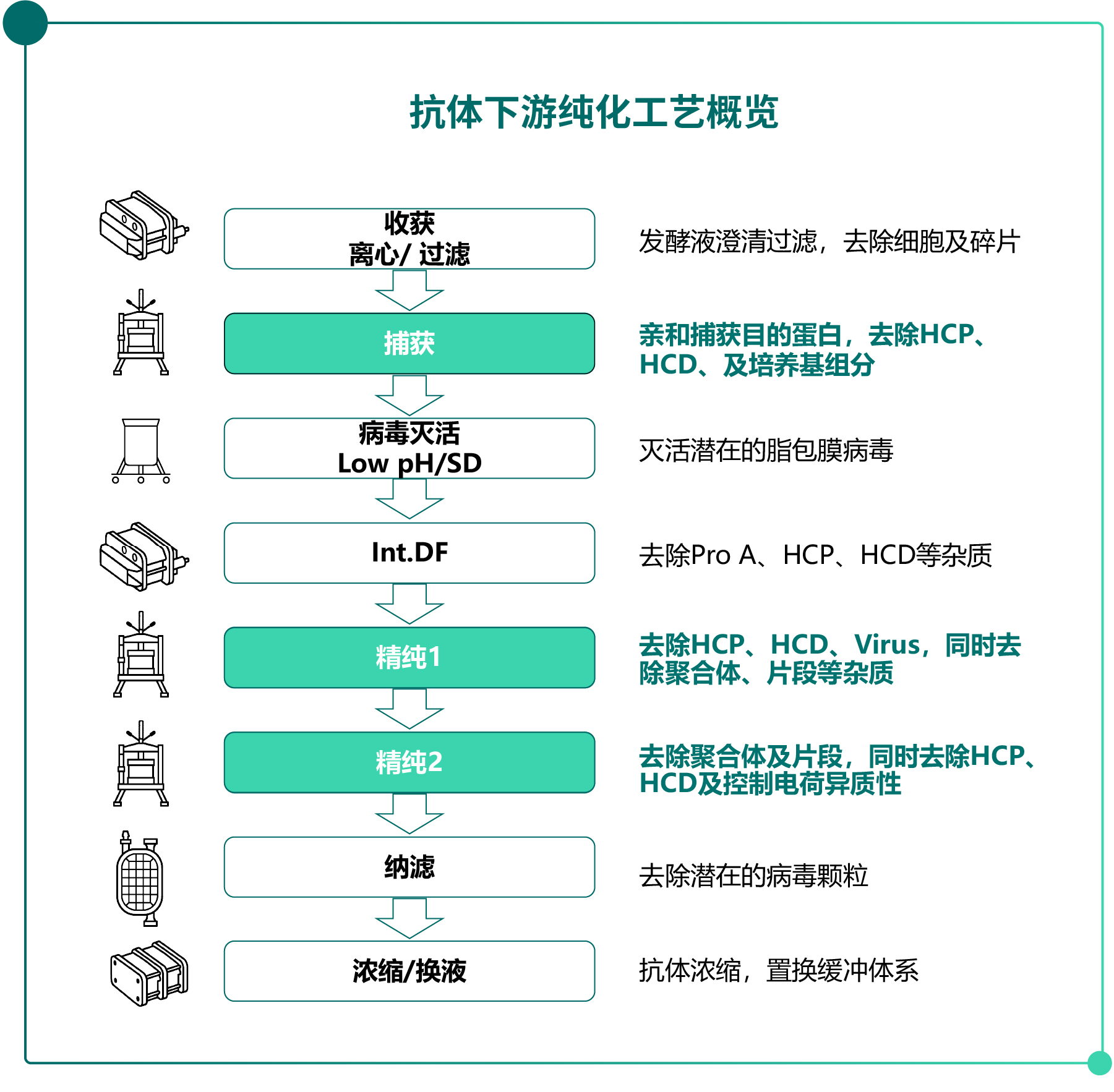
Fig.4 抗体纯化的典型流程
3. 抗体纯化捕获介绍
抗体纯化的捕获阶段是通过抗体亲和层析来完成的。抗体亲和层析(Antibody Affinity Chromatography)是利用生物分子间特异性相互作用实现高选择性分离的经典方法。
最常用的配基为 Protein A——源自金黄色葡萄球菌的膜蛋白,可与抗体 Fc 区特异性结合,实现一步捕获与高纯化。
(1) protein A亲和层析
(2) 天然 Protein A 含五个同源的IgG结合区域(E、D、A、B、C),但全长分子含非特异结合片段。因此现代商业化填料多采用基因改造型Protein A,显著降低非特异性吸附并大幅提升耐碱性。此外,Protein A的结构域还可以与Fab片段的VH区域结合。这些结合作用包括疏水作用、氢键和盐桥。
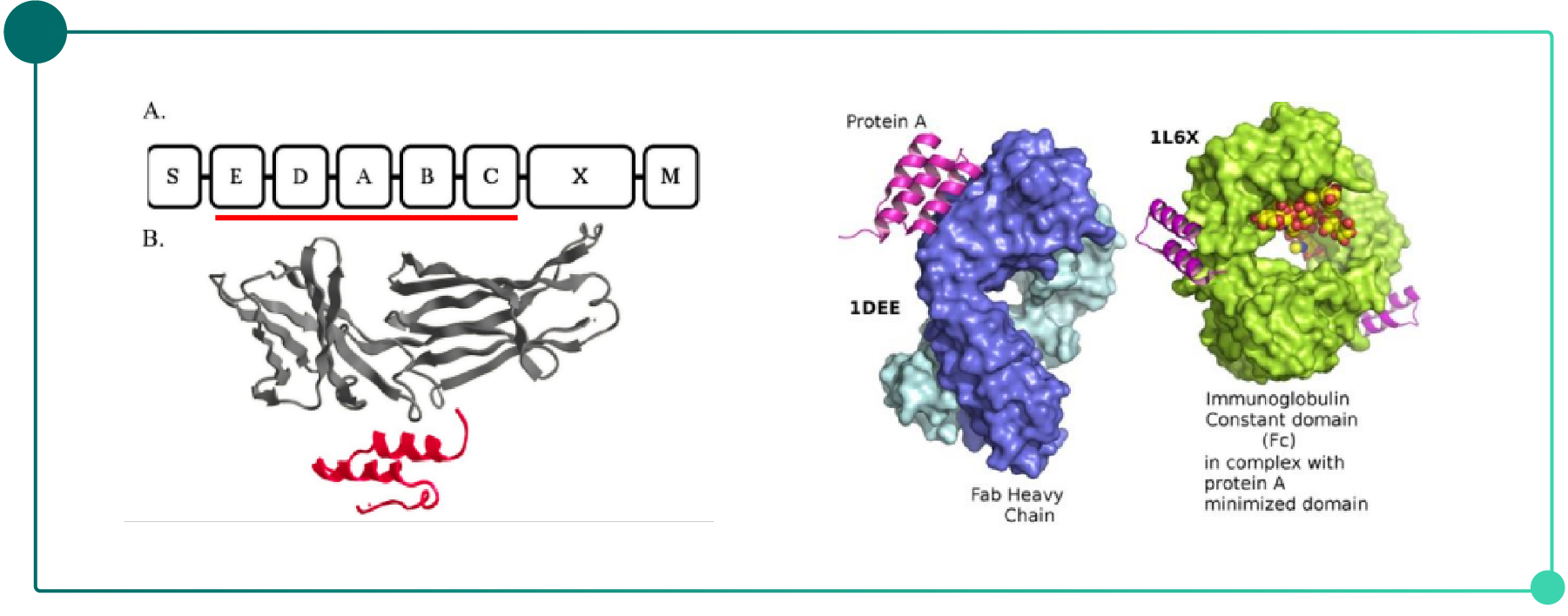
Fig.5 protein A亲和层析结合原理
(3) 其他抗体亲和层析
此外,对于 Fab、IgM、抗体片段 等特殊分子,还可使用 Protein L(结合 κ 链)或 IgM 亲和填料进行特异分离。
4. 抗体纯化精纯介绍
经过抗体捕获层析,即亲和层析后,抗体蛋白纯度通常在90%以上,HCP、HCD杂质含量明显降低,但仍需在后续步骤进行去除;另外,对产品相关杂质如聚体、片段、电荷异构体等以及因亲和捕获引入的配基如rProA 杂质的去除,需要进一步的精纯层析步骤,如IEX、MMC/MMA、HIC和GF。

(1) 阴离子交换层析(AEX)——流穿模式
这是抗体精纯中最常用的操作模式,主要去除HCP、HCD、Virus等大部分工艺相关杂质,也可归为中度纯化。
(2) 阳离子交换层析(CEX)——结合/洗脱模式
阳离子层析通常采用结合洗脱模式,可以去除HCP、HCD和聚体、片段、电荷异构体等产品相关杂质。
(3) MMC/MMA——结合洗脱或流穿模式
复合模式层析结合了离子交换作用和疏水作用两种分离原理,可以采用结合洗脱或流穿模式,用以去除聚体、片段等产品相关杂质,和/或HCP、HCD、内毒素、病毒等杂质。
(4) HIC——流穿/结合洗脱
当离子交换无法有效去除聚集体时,HIC可作为补充或替代方案。疏水层析常采用流穿或结合洗脱模式,用于去除HCP、聚体、片段等杂质。
(5) GF——流穿/结合洗脱
凝胶过滤层析为非吸附层析,通过目的蛋白与其他杂质的分子大小差异来进行分离。层析过程操作简单,可用在精细纯化的最后一步,也可用于对样品进行脱盐换液。因其精细分离上样量少,大生产中一般会尽量避免使用。
四、抗体纯化过程中常见的问题及应对方法
1. 目标蛋白不结合或结合效率低?
• 填料失活:配基(如Ni²⁺、抗体等)因反复使用、清洗不当或保存不当失去活性。
• 样品问题:1)样品粘度太高。2)样品中含有高浓度的竞争性物质(如IMAC中的咪唑、高浓度DTT会还原金属离子)
• 缓冲液条件不当:1)pH值:超出蛋白或配基的稳定范围。2)螯合剂:在IMAC(如镍柱)中,缓冲液中含有EDTA等螯合剂,会剥落柱子的金属离子。
• 流速过快:蛋白与配基没有足够的接触时间进行结合。
• 标签问题(针对标签蛋白纯化,如His-tag):1) 标签未成功表达或表达不完全。2)标签被屏蔽(例如,在包涵体中或由于蛋白高级结构)。
2. 如何去除Protein A亲和填料吸附的色素?
色素性质复杂,可根据填料的耐受情况制定CIP方案。NaOH是最常用的清洁试剂。除此之外,高盐、有机试剂(20%乙醇或30%异丙醇)、尿素、盐酸胍或酸也是常见的清洗方案。也可通过混合试剂或其他针对性清洗方法对填料进行处理,如已知色素种类,可根据色素的性质采用特定的方法进行清洗。
3. Protein A亲和填料提高产品纯度的方法?
• 改变样品中盐浓度或优化pH值
• 增加洗杂步骤(高盐或有机溶剂)
• 优化洗脱pH 值
4. 离子交换层析精纯时目标蛋白不能很好地与其他杂质峰分开?
可能原因包括洗脱梯度不合适,可以选择更缓一些的洗脱梯度,也可能是流速太快,或者是蛋白在洗脱过程中发生聚集等。也可以更换分辨率更高的产品。
5. 蛋白不结合离子填料?
样品不结合可能是盐浓度太高或者pH不合适,也可能因为buffer中含有带电物质(如去垢剂等)以及柱效下降等原因。可以检查柱效、优化上样条件等解决。
6. 疏水层析时目的蛋白洗脱峰早,分辨率差
建议提高平衡及样品盐浓度或使用更强盐析作用力的盐;如果依然没有改善可以尝试其它的配基、
或高配基密度的疏水填料进行测试。
结语
抗体纯化是一门平衡“分辨率、载量、速度、回收率”与“成本”的工艺科学。从抗体分子的结构与分类出发,深入理解不同层析技术的原理与适用场景,科学设计捕获与精纯策略,是构建高效、稳健的抗体纯化工艺的关键。
随着抗体药物分子形式日趋多样化(双抗、ADC、AOC等),传统平台化纯化工艺面临新的挑战。Protein A结合差异增大、分子稳定性更敏感、杂质性质更接近等问题,对配基选择、洗脱条件及清洗策略提出更高要求。未来,开发兼顾高载量、高选择性、温和洗脱条件的亲和填料,将是抗体纯化工艺发展的重要方向。





.png)


